Cerdanyola del Vallès, 31 d'octubre de 2018 Investigadors de l'Institut de Biologia Molecular de Barcelona (IBMB-CSIC) i de l'Institut de Biotecnologia i Biomedicina (IBB-UAB) han descobert el mecanisme pel qual el bacteri Mycoplasma genitalium (Mge) s'adhereix a les cèl·lules humanes. Aquesta adhesió és essencial per a l'establiment de la infecció i el posterior desenvolupament de la malaltia.
Mge és un patogen emergent responsable de diverses infeccions genitourinàries. En homes, és una de les principals causes d'uretritis (15-20%) i en dones, s'ha associat a quadres de cervicitis, malaltia inflamatòria pèlvica, part prematur i avortament espontani. Fins ara se sabia que l'adhesió del bacteri al tracte genitourinari té lloc per mitjà d'unes proteïnes, denominades adhesines, que reconeixen receptors específics en la superfície de les cèl·lules.
En aquest estudi, els investigadors de l’IBMB-CSIC han determinat l'estructura tridimensional de l’adhesina P110 d’Mge unida a aquests receptors cel·lulars mitjançant difracció de raigs X amb cristal·lografia de proteïnes a la línia de llum XALOC. "Hem fet cristalls que contenien l’adhesina P110 unida al receptor i els hem difractat amb els raigs X del sincrotró, la qual cosa ens ha revelat la posició exacta dels àtoms en la proteïna i hem pogut definir l'estructura en tres dimensions", explica David Aparicio, investigador de l'IBMB.
Paral·lelament, científics de l'IBB-UAB han realitzat estudis in vivo amb cèl·lules humanes i han demostrat que mutacions en llocs concrets de la proteïna P110 impedeixen la unió d’Mge. Aquests resultats han permès confirmar la informació derivada de l'estructura tridimensional obtinguda.
Els resultats permeten entendre les bases moleculars de la unió d’Mge amb les cèl·lules humanes. "D'una banda, hem aconseguit informació clau sobre el procés de colonització, és a dir, la presa de contacte del patogen amb les cèl·lules de l'hoste. De l'altra, això ens permet desenvolupar fàrmacs alternatius als antibiòtics capaços de bloquejar l'adhesió d’Mge a les cèl·lules, com molècules que mimetitzin els receptors cel·lulars, o que estimulin la formació d'anticossos que inhibeixin la funció de les adhesines", explica Oscar Quijada, investigador de l'IBB.
La investigació ha propiciat la sol·licitud d'una patent internacional i s'ha iniciat una col·laboració amb el servei i el grup de recerca en microbiologia del Campus Vall d’Hebron amb l’objectiu de lluitar contra l'aparició de resistències.
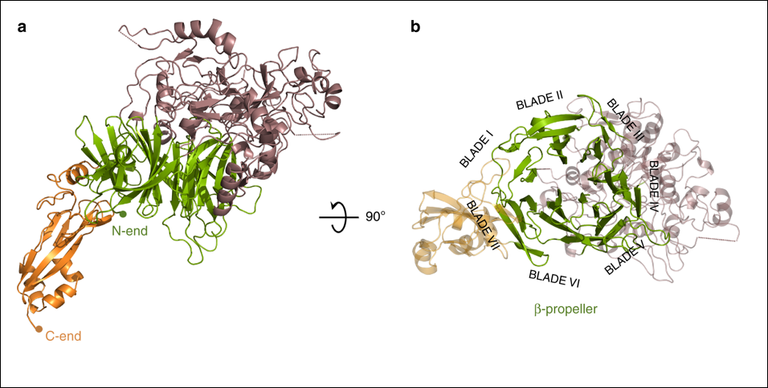
Estructura general de P110. Dues vistes, separades 90º entre sí, de la regió extracel·lular de P110 que està formada per un gran domini N, amb una hèlix β de set pales (verd), la corona (marró) i el domini C (taronja). En la part lateral dreta, la vista és al llarg de l'eix central de l'hèlix β. La situació de les set pales en l'hèlix s'indica explícitament i mostra que les dues pales terminals I i VII estan prop del domini C-terminal i oposades a la corona. Imatge de Nature Communications, D. Aparicio, S. Torres-Puig, M. Ratera, E. Querol, J. Piñol, O.Q. Pich i I. Fita.
La resistència a antibiòtics
Actualment, les infeccions d’Mge són tan freqüents com les de gonorrea, una de les infeccions de transmissió sexual més conegudes. A més, Mge s'està convertint en un superbacteri resistent a tots els antibiòtics disponibles actualment, fet que aviat ens deixarà sense alternatives terapèutiques. La resistència a antibiòtics és un problema cada vegada més prevalent. Mitjançant canvis genètics, molts bacteris han desenvolupat la capacitat de resistir als antibiòtics i continuar reproduint-se. Tot i que és un procés natural, el mal ús i l'abús d'aquests medicaments està accelerant el procés. Atès que Mge està desenvolupant resistència a tots els antibiòtics disponibles, trobar una estratègia terapèutica alternativa és especialment rellevant. Els resultats obtinguts són essencials per al disseny de nous fàrmacs, ja que permeten definir l'adhesió a escala molecular.
Referència: David Aparicio, Sergi Torres-Puig, Mercè Ratera, Enrique Querol, Jaume Piñol, Oscar Q. Pich, and Ignacio Fita. Mycoplasma genitalium adhesin P110 binds sialic-acid human receptors. Nature Communications. DOI 10.1038 / s41467-018-06963-i
Article original Universitat Autònoma de Barcelona




